- ۱۳۹۷ ۳۰ خرداد
سوسپانسيونها، امروزه كاربردهاي وسيعيی در صنايع مختلف مانند لاستيك، رنگ، چسب، افزودنيهاي كاغذ و منسوجات، اصلاح چرم و افزودنيهاي مواد ساختماني دارند. همينطور از آنها در پزشكي و كاربردهاي وابسته به داروها و سيستمهاي تحويل دارو استفاده ميشود. به دليل مسائل محيط زيستي و قانونهاي تصويب شده براي جايگزين كردن سيستمهاي پايه حلالي با محصولات سازگار با محيط زيست و پايه آبي، اين سيستمها به سرعت گسترش پيدا كردند. چون سوسپانسيونهاي پليمري خواص و ويژگيهاي منحصر به فردي دارند كه آنها را براي استفاده در بسياري از بازارها مناسب كرده است.
اين محصولات معمولا به روش پليمريزاسيون امولسيوني سنتي تهيه ميشوند. در اين فرايند، منومر در محلولي از Surfactant در آب با غلظت كمي بيشتر از CMC پخش ميشود و پليمريزاسيون با سيستمهاي آغازگر (كه معمولا در فاز آبي قابل حل ميباشند)، شروع ميشود. ذرات پليمري با ورود راديكالها به درون مايسلها (هسته سازي هتروژن)، رشد اليگومرها در فاز آبي (هسته سازي هموژن) و ورود راديكالها به قطرات منومري حاصل ميشوند. اندازه قطرات منومري در حدود 1 تا 10ميكرون است و در مقابل اندازه منومرهاي وارد مايسل شده كه اندازهاي در حدود 10 تا 20 نانومتر دارند، نسبتا بزرگتر هستند و در نتيجه مساحت سطح (Surface area) مايسلها به مراتب از قطرات پليمري بيشتر است. بنابراين احتمال ورود راديكال آزاد به درون قطرات منومري بسيار اندك است و هسته سازي بيشتر به روشهاي هتروژن و هموژن انجام ميشود. هنگامي كه هسته سازي انجام شد، ذرات پليمري با واكنشهاي پليمريزاسيون تشكيل ميشوند. منومر مورد نياز براي ادامه پليمريزاسيون بايد از طريق نفوذ آنها از قطرات منومري در محلول آبي تامين شود و در برخي موارد اين مكانيزم محدوديتهايي براي پليمريزاسيون امولسيوني ايجاد ميكند. مثلا در برخي موارد متصل كردن منومرهاي آبگريز مانند لوريل و استريل متاكريلاتها به زنجيره اصلي پليمر باعث بالا رفتن مقاومت در برابر آب، در فيلم حاصل از پليمر سوسپانسيون شده ميشود. اما انتقال جرم اين مواد از قطرات پليمري در محلول آبي شديدا تحت كنترل پديده نفوذ است. بنابراين در پليمريزاسيون امولسيوني امكان استفاده از آنها وجود ندارد. اگر همهي قطرات منومري و يا حداقل درصد قابل توجهي از آنها تبديل به هسته شوند، نياز به انتقال جرم منومرها در محلول آبي به حداقل ميرسد و اين زماني رخ ميدهد كه مساحت سطح قطرات منومري بزرگ و قابل مقايسه با مايسلها باشد و اين مستلزم داشتن اندازه ذرات زير ميكرون و در حد نانو است. واژه مينيامولسيون براي ديسپرسيون روغن در آب به اندازه ذرات زير ميكرون است كه براي مدتي، از چندين ساعت تا چندين ماه پايدار است.
توليد و به كار بردن نانو ذرات پليمري كه در يك محمل غير آلي پخش شده اند و به لاتكس هاي پليمري معروفند، در علم پليمر يك رنسانس به وجود آورده است. و اين به چند دليل است. از يك طرف به دليل مسائل امنيتي، بهداشتي، زيست محيطي و مسائل مربوط به سلامت، گرايش به فرمولاسيون پليمرها در حلالهاي سالم و غير آلي كه آب در راس آن ها قراردارد، بيشتر شده است و به همين دليل علم پليمر بايد با مشكلات پخش و توليد پليمرها در آب (علي رغم اين كه ممكن است آب در فرايند پليمريزاسيون مشكل ايجاد كند) مقابله كند. دليل دوم براي گسترش اين مساله، گرايش به توليد فرمولاسيون پليمرها با درصد جامد بالا است كه در نتيجه اثرات مربوط به Shrinkage به حداقل ميرسد و زمان فرايند هم كم ميشود. توليد يك پليمر با درصد جامد بالا و در عين حال ويسكوزيته قابل قبول و مناسب فقط با ديسپرسيونهاي پليمري در آب و يا در حلال هاي آلي ميسر است. سوم اين كه دانشمندان فهميدهاند كه با ديسپرسيون هاي پليمري و مثلا با تنظيم اندازه ذرات، ميتوانند خواص بيشتري را به توده پليمري اضافه كنند. يعني ميتوانند خواصي را ايجاد كنند كه فقط مربوط به طراحي ساختار مولكولي پليمر نيست. مثلا توليد لاستيكهاي بهتر و يا ترموپلاستيك هاي مقاوم در برابر شوك. بيشتر لاتكسهاي پليمري با پليمريزاسيون امولسيوني تهيه ميشوند. با وجودي كه پليمريزاسيون امولسيوني گسترش باور نكردني و كاربردهاي فراواني دارد، از برخي جهات محدوديت هايي هم دارد. و آن اين كه واكنش هاي پليمريزاسيون محدودي هستند كه به اين روش قابل انجام هستند. پليمريزاسيون امولسيوني براي هموپليمريزاسيون راديكالي دسته محدودي از منومرهاي محلول در آب خوب است اما محدوديتهاي عمدهاي در كوپليمريزاسيون راديكالي و واكنشهاي ديگر پليمرها دارد. علت اين امر، مكانيزم اين پليمريزاسيون است كه ذرات پليمري كه حاصل اين نوع پليمريزاسيون هستند و با سينتيك كنترل ميشوند، همه از مركز به سمت سطح ساخته ميشوند و تمام منومرها بايد توسط نفوذ در فاز آبي انتقال يابند. بنابراين حتي در پليمريزاسيون راديكالي معايبي هم چون نقص در يكنواختي و عدم توانايي به دستيابي به تركيبهاي مورد نظر وجود دارد.
روشهاي ديگري هم براي توليد ديسپرسيون هاي پليمري مانند پليمريزاسيون ميكروامولسيونها، پليمريزاسيون سوسپاسيوني و ... وجود دارند كه هر كدام نقايصي همچون استفاده زياد از Surfactantها، كم بودن پايداري كلوئيدي و يا گراني فرايند دارند كه جلو استفاده وسيع آنها را در علم پليمر ميگيرد. مفهوم ايده آلي در پليمريزاسيون هتروژن وجود دارد كه در آن قطرات كوچك يكنواخت و پايدار منومر و يا اليگومر وجود دارند. و بدون اين كه خواص مطلوب خود را از دست بدهند و يا روي سينتيك تاثير نامطلوبي بگذارند به پليمر تبديل شوند. يعني قطرات منومري، محل شروع واكنشهاي پليمريزاسيون شوند.
تفاوتهاي بين پلیمریزاسیون ماكروامولسيون، مينيامولسيون، ميكروامولسيون و پليمريزاسيون سوسپانسيوني
مينيامولسيون در تعريف، فقط به اندازه ذرات محدود نميشود، بلكه مكانيزم و عملكرد آن هم متفاوت است. بنابراين در بسياري موارد ميتوان مينيامولسيون را از ساير روشهاي پليمريزاسيون هتروژن تفكيك كرد. شكل زیر تا حدودي اين مكانيزمها را نشان ميدهد. پليمريزاسيون در ميكروامولسيونها در حالت تعادل ترموديناميكي شروع ميشود كه توسط مقادير زيادي از مواد و يا سيستمهاي مواد فعال سطحي فراهم ميشود. و كشش سطحي حد فاصل روغن و آب به صفر نزديك است. در مقابل، مينيامولسيونها به سختي پايدار ميشوند و برش و نيروي زيادي براي رساندن آنها به حالت پايدار لازم است و كشش سطحي حد فاصل، بسيار بيشتر از صفر است. مقادير زيادي از Surfactant كه در ميكروامولسيون ها به كار ميرود، تمام سطح ذرات را پوشش ميدهد. از آن جايي كه واكنشهاي شروع نميتوانند به طور همزمان در همهي قطرات صورت گيرند، زنجيرههاي پليمري اوليه، تنها در برخي از قطرات شكل ميگيرند. اثرات فشار اسمزي و الاستيكي اين زنجيرهها ميكروامولسيونهاي ضعيف را ناپايدار ميكند و معمولا منجر به افزايش اندازه ذرات، تشكيل مايسلهاي خالي و هسته سازی نوع دوم ميشود. محصول نهايي، لاتكسهاي بسيار ريز به اندازه ي 5-50 نانومتر است كه با مقادير زيادي از مايسلهاي خالي همزيستي ميكنند.
در پليمريزاسيون امولسيوني قطرات منومر بزرگ كه با Surfactant پايدار شدهاند و مايسلهاي خالي يا منومرهاي وارد مايسل شده، وجود دارند و پليمريزاسيون ميتواند در همه ي آن ها شروع شود. شروع كنندههاي محلول در آب، اليگوراديكالهايي با حلاليت كم در آب تشكيل ميدهند و اين تا زماني ادامه مييابد كه آنها به اندازهي كافي آبگريز شوند تا بتوانند وارد مايسلها شوند و يا در فاز پيوسته تشكيل هسته بدهند در خلال پلمريزاسيون، منومرها از قطرات بزرگ منومري براي تغذيه مايسلها در فاز آبي ادامه نفوذ ميكنند تا زماني كه قطرات ناپديد شوند. ذراتي به اندازه معمولا بزرگتر از 100 نانومتر تشكيل ميشوند. با توجه به افزايش مساحت حد فاصل، با پليمريزاسيون كشش سطحي لاتكس افزايش مييابد. در پليمريزاسيون امولسيوني اندازه ذرات لاتكس به اندازه قطرات اوليه امولسيون وابسته نيستند و اندازه آنها توسط فاكتورهاي سينتيكي مانند: دما، مقدار شروع كننده، سرعت توليد هسته ها و پايداري نانوذره ها اثر ميپذيرد. اين فاكتورها در مينيامولسيون بياثرند و ذرات لاتكس همان ذرات قطرات منومري اوليه هستند كه پليمريزه شدهاند و اندازه آنها وابسته به فرآيند ديسپريونسازي و مستقل از پارامترهاي پليمريزاسيون است.

پليمريزاسيون سوسپانسيوني شامل قطرات بزرگتري از منومر (1ميكرون تا 1 ميليمتر) است كه در فاز پيوسته پخش شده است. هسته سازي غالبا در قطرات انجام ميشود و هر قطره به صورت يك رآكتور بچ مجزا عمل ميكند و بسيار شبيه مكانيزم مينيامولسيون است و تفاوت اصلي در سايز و پايداري ذرات تشكيل شده است. در اين نوع پليمريزاسيون، هسته سازي در قطرات منومري انجام ميشود و متوسط راديكالها به ازاي ذرات، بسيار زياد است (106-102). با توجه به اندازه ذرات بسيار بزرگ، فشار قطرات كم است و Ostwald ripening با سرعت بسيار كمتري صورت ميگيرد و به همين دليل است كه افزودن آبگريز در پليمريزاسيون سوسپانسيوني معمول نيست.
كارهاي اخير
براي اولين بار Ugelstad نشان داد كه با كوچك شدن اندازه قطرات به اندازه كافي، مكانيزم تشكيل هسته قطرهاي بيشتر ميگردد و نشان داده شد كه الكلهاي چرب با زنجيره بلند، قابليت Surfactantهاي آنيوني را در پخش و پايدار كردن ديسپرسيونهاي روغن در آب افزايش ميدهد. گزارش شد كه الكلهاي چرب انرژي بين سطحي را كاهش ميدهند و باعث ميشوند كه ذرات به اندازه دلخواه كوچك شوند. Ugelstad،Cetyl alcohol (CA) را با Sodium luryl sulfate (SLS) در آب مخلوط كرد و استايرن را در حال به هم زدن و در دماي 60 درجه سلسيوس به آن افزود و مشاهده كرد كه مينيامولسيون براي مدت دو هفته پايدار ماند. واكنش را در همان دما شروع كرد و مشاهده شد كه هنگامي كه مقدار كمتري از مواد فعال سطحي به كار ميرود، ذرات پليمري بيشتر از هسته سازي قطرهاي حاصل ميشوند. قبلا هم Ugelstad پايدار سازي امولسيون vinyl Chloride را با مخلوطي از Surfactant آنيوني و الكلهاي چرب پيشنهاد كرده بود.
كارهاي جديدي در مورد فرموله كردن و پايدار سازي امولسيونها انجام شد. Ugelstad مخلوط hexadecanol/Sodium hexadecyl sulfate را در آب 70 درجه سلسیوس فراهم كرد. مخلوط را تا دماي 60 درجه خنك كرد و بعد منومر استايرن را در 600 rpm به آن افزود و فهميد كه اندازه ذرات كاهش پيدا كرد و در نسبت Surfactant به الكل 1 به 3 پايداري افزايش پيدا كرد. مينيامولسيون با گذشت زمان افت ميكرد و اين افت در دماهاي بالاتر شديدتر بود. مكانيزمي كه براي امولسيون سازي پيشنهاد شد اين بود كه يك كمپلكس موقتSurfactant/الكل چرب، تشكيل ميشود كه به امولسيفاي كردن منومر كمك ميكند. سپس الكل چرب به درون قطره نفوذ ميكند و پايداري قطره را از بين ميبرد. بر اساس اين مكانيزم، مقدار الكل چرب بايد از طرفي به اندازهاي كم باشد كه پايداري قطره را به هم نزند و از طرفي به اندازهاي باشد كه برای انجام وظيفهاش در امولسيون سازي و تشكيل كمپلكس كافي باشد. اين مكانيزم با آزمايشي تاييد شد. و آن اين بود كه الكل چرب از قبل در منومر استايرن حل شد و نتيجهاش چيزي جز سيستم هاي ناپايدار نبود. به هر حال مكانيزم بر اين پايه استوار بود كه وظيفه الكل چرب تنها اصلاح سطح قطره است و بعدها نشان داده شد كه درست نيست. در مينيامولسيون سازي استايرن دو نوع توزيع اندازه ذره وجود داشت كه ذرات بزرگ مربوط به هسته سازي قطرهاي بود. الكلهاي چرب باعث كم شدن انرژي بين سطحي شده، باعث ميشوند كه اندازه ذرات مناسب حاصل شوند. بنابراين فقط در نسبت هاي بالاي الكل چرب به Surfactant، هسته سازي حاصل شد. الكلهاي چرب راCosurfactant ناميدند. Azad فهميد كه الكلهاي چرب با زنجيره هاي طولاني تر پايداري را بيشتر ميكنند. او و همكارانش با الهام از كار آقايان Hallworth و Carless و همچنين Smith و Davies كه گزارش كرده بودند كه امولسيون نفت سبك، بنزن و هگزان با افزودن مقدار كمي hexadence (HD) به شدت افزايش مييابد، تصميم گرفتند از HD در مينيامولسيون كردن منومرها به جاي الكل هاي چرب استفاده كنند. در آغاز مشاهده كردند كه با دستگاههاي همزن معمولي به سرعتي كه به وسيلهي الكلهاي چرب با زنجيره طولاني ميشود، به امولسيون نميرسند. بنابراين از سيستمهاي هموژنايزر با كارايي بالاتر استفاده كردند و با هموژنيزه كردن يك امولسيون حاوي HD با يك دستگاه هموژنايزر فشار بالاي آزمايشگاهي به يك مينيامولسيون به شدت پايدار رسيدند. هموژنيزه كردن مينيامولسيون حاوي الكل چرب اثري بر روي پايداري آن نداشت اما در اين مورد پايداري امولسيون، مستقل از طريقهي مخلوط كردن آنها (اختلاط اولیه) است. Misra و Higushi براي اولين بار بيان كردند كه ناپايداري در امولسيون ها به خاطر اثر نفوذ مولكولي (Ostwald ripening effect) است. اين نظريه بر اين پايه است كه پتانسيل شيميايي قطرات منومري كوچكتر، به خاطر اثرات انرژي سطحي، بيشتر از قطرات منومري بزرگتر و يا سطوح صاف است. بنابراين منومر از قطرات كوچكتر به قطرات بزرگتر نفوذ ميكند كه نتيجه آن بزرگتر شدن قطرات و ناپايدار شدن سيستم است. آنها پيشبيني كردند كه افزودن كمي از مواد نامحلول، ميتواند افت (degradation) امولسيون به خاطر اثرات نفوذ مولكولي را به تاخير اندازد. چون سرعت نفوذ كم مواد نامحلول از تعادل منومرها در بين قطرات جلوگيري ميكند و بنابراين تاخير در پايداري سيستم منوط به تغيير در توزيع جزء، با كمترين سرعت نفوذ است. Smith و Davies اثر مقدار كمي از hexadence در جلوگيري از افت مينيامولسيون را به همين اثرات گفته شده در بالا نسبت دادند. Dubrin درجات مختلف امولسيون سازي را بررسي كرد و به اين نتجه رسيد كه در يك سيستم استايرن- سرفكتانت آنيوني- آب، بدونCA يا HD هسته سازي قطرهاي بسيار كم است. كار اخير اساس فرآيند پليمريزاسيون مينيامولسيوني را بنا كرد. يعني بايد هموژنيزه كردن با انرژي بالا براي كاهش اندازه ذرات اعمال شود و قطرات توليد شده با استفاده از يك جزء نامحلول در آب و يك Surfactant مناسب از لخته شدن و اثرات Ostwald ripening حفظ میشوند. اين كار حتي نامگذاريها را هم تحت تاثير قرار داد. مثلا در مراجع پليمريزاسيون مينيامولسيوني، اجزاء نامحلول در آب و با وزن مولكولي پايين معمولا به Cosurfactant ياد ميشوند. اما به جز الكلهاي با زنجير بزرگ، تركيباتي مثل hexadence فعاليت سطحي ندارند. به علاوه اثر اصلي اين تركيبات در پايدار سازي، اثر در بالك است و نه در سطح. مادهاي كه قطرات را در برابر نفوذ مولكولي حفظ ميكند، به خاطر خاصيت نامحلولي، آبگريز (hydrophobe) هم ناميده ميشود. با اين كه هر تركيب نامحلول درآب ميتواند Ostwald ripening را به تاخير بيندازد، اما توانايي آن به شدت وابسته به وزن مولكولي آن است. يعني مواد نامحلول در آب با وزن مولكولي كم، از اين مواد با وزن مولكولي بالا بازده بهتري دارند. به علاوه استفاده از اسم آبگريز، محدود به مواد نامحلول با وزن مولكولي بالا (مانند پليمرها) است. بنابراين نام Costabilizer نامي است كه براي اجزاي نامحلول در آب با وزن مولكولي كم به كار ميرود.
اثرات مواد فعال سطحی (Surfactant)
پايداري كلوئيدها معمولا با انتخاب نوع و ميزان Surfactant كنترل ميشود. ما در اين جا مطالب كلي را در مورد يك Surfactant نمونه (SDS) بيان ميكنيم. در مينيامولسيونها سرعت اختلاط تعادل موقع هم زدن و بنابراين اندازه قطرات بلافاصله بعد از به تعادل رسدن به ميزان امولسيفاير بستگي دارد. براي سيستم استايرن و SDS يك بازه از 180 نانومتر (3/0% وزنی SDS نسبت به استايرن) تا 32 نانومتر (50% وزنی SDS نسبت به استايرن) وجود دارد.
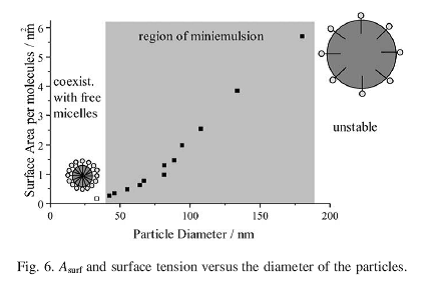
در مقايسه با پليمريزاسيون ميكروامولسيوني و امولسيوني اين اندازه ذرات نسبت به Surfactant مصرف شده بسيار خوب است. يك لاتكس به اندازه ذرات 32 نانومتر نيمه شفاف است و بسيار نزديك به نتیجه پليمريزاسيون ميكروامولسيوني است و بدون استفاده از آبگريز و با استفاده از مخلوط الكل/SDS به دست آمده است. براي مطالعهي بازدهي Surfactant و چگونگي پيشرفت واكنش نسبت به اندازه ذرات،Asurf تعریف شده كه عبارت است از متوسط مساحت روغن پايدار شده در آب به ازاي يك مولكول Surfactant كه بستگي شديدي به اندازه ذرات دارد. يعني براي ذرات كوچك يك لايه انبوه از Surfactant، تمام ذره را پوشش ميدهد و براي ذرات بزرگ لاتكس، اين پوشش كامل نيست. اين یعني ذرات كوچكتر جزء حجمي قابل توجهي دارند، متوسط فاصله سطح به سطح كمتري دارند، حركت نسبي بيشتر و پتانسيل كمتري دارند و بنابراين لايهي بزرگتري از Surfactant را روي خود جاي ميدهند. از آن جا كه لايه غليظ روي ذرات، شيمي برخي چيزها مانند سرعت نفوذ به طرف سطح و يا زياد شده تركيبات قطبي در داخل قطره، با توجه داشت كه در برخي موارد اندازه قطرات بزرگ بهتر است.
مقادير Asurf در حدود 2/0 nm2 مقادير زياد Surfactant را نشان ميدهد و در نتيجه مايسل هاي خالي وجود دارند و يا چند لايه روي ذرات جذب شده است كه براي مينيامولسيون ايجاد مشكل ميكند و از ناحيه ايده آل آن خارج ميشود و از طرف ديگر استفاده از مقادير كمتر از 3/0% از Surfactant، كلوئيد ناپايدار حاصل ميكند و باز هم از ناحيهي ايده آل آن خارج ميشويم. قابل ذكر است كه اثر پوشش دهيSurfactantها، در كشش سطح هاي مختلف لاتكس ها متفاوت است. پلي استايرن بر پایه سنتز مينيامولسيوني، كه داراي اندازه ذراتي در حدود 100 nm است، كشش سطحي در حد آب خالص دارد. اين به اين خاطر است كه اندازه ذرات به قدري بزرگ است كه جذب تعادلي باعث ميشود كه كمي Surfactant آزاد باقي بماند. قطرات كوچكتر بيشتر پوشيده ميشوند و غلظت تعادلي Surfactant آزاد بيشتري را ايجاد ميکنند و البته این غلظت بيشتر، باز هم به خوبي زير CMC است. به زبان ديگر در مينيامولسيونها، مايسل آزاد وجود ندارد و اين در واكنش پذيري شيميايي و سرعت پليمريزاسيون بسيار مهم است. اما در غلظتهای بيشتر (50% SDS)، مايسلها ديده ميشوند كه ميتوان آن را مينيامولسيون به حساب نياورد.
نوع Surfactant
بيشتر توضيحات داده شده، بر پايه استفاده از Surfactant آنيوني SDS است. براي اولين بار در سال 1976 استفاده از Surfactantهاي كاتيوني (مانند octadecyl pridinium bromide) براي تهيه مينيامولسيون ها شروع شد. وقتي براي تهيه مينيامولسيونها ازSurfactantهاي كاتيوني استفاده ميشد، نتيجه امولسيونهايي با توزيع اندازه قطرات پهن بود. EL-Aassar از آنها براي تهيه ي مينيامولسيونها هم اسفاده كرد. كار اخير بر روي مينيامولسيونهاي حالت پايدار كه از Surfactantهاي كاتيوني استفاده كرده، منجر به تهيه لاتكسي پايدار با توزيع اندازه ذرات باريك شد. نتايج اندازه گيريهاي كشش سطحي، ميزان پوشش دهي 30 درصدي قطرات را نشان ميداد كه حاكي از بازده خوب اين Surfactantها است. گونه جديدي از Surfactantهاي كاتيوني با گروههاي سولفوني هم در تهيه ي ميني امولسيونها به كار رفته اند.
براي توليد مينيامولسيونهاي غير يوني ميتوان از 3 تا 5 درصد از مشتقات poly(ethelene oxide) استفاده كرد. اگر چه اندازه ذرات بزرگتر ميشود اما پايداري بالا است. Chern و Liou از Surfactant غير يوني nonylphenol polyethoxylate استفاده كردند و اندازه ذرات بين 135 تا 280 نانومتر حاصل شد. گزارش شد كه اندازه ذرات، بيشتر به مقدار و نوع آبگريز و اثر Ostwald ripening بستگي دارد. Capek از ماكرومنومرها در مينيامولسيونها استفاده كرد. Chern و Liou از HD به عنوان آبگريز و از poly(methyl methacrylate-b-(diethylamino)ethyl methacrylate) به عنوان Surfactant استفاده كردند و اندازه ذرات بين 150 و 400 nm حاصل شد. در پايدار سازي وينيل استات مي توان از PVOH به عنوان Surfactant غير يوني و HD به عنوان آبگريز استفاده كرد. Basker در كاري بسيار جالب در توليد پلي استايرن از كوپليمر Octadecyl acrylate و آكريليك يا متاكريليك اسيد استفاده كرد كه نقش Surfactant و آبگريز را با هم ايفا ميكند و به لحاظ اقتصادي بسيار مهم است. چون كوپليمر نه در آب و نه در منومر به خوبي حل نميشود و مجبور است كه در حد فاصل روغن و آب قرار بگيرند. با تغيير ميزان Surfactant نسبت به منومر ميتوان اندازه ذرات را در بازه زيادي جابجا كرد. شكل زیر، بستگي نوعSurfactant و اندازه ذرات را نشان ميدهد. لاتكسهاي حاصله از SDS و cetyltrimethyl ammonium bromide، مستقل از نوع بار كارايي يكساني را نشان ميدهند. بازده Surfactantهاي غير يوني كمتر است و نمودارهاي آنها كلا به درجات بالاتر انتقال يافته اند.Polydispersity هم براي سيستمهاي غير يوني پهن تر است.
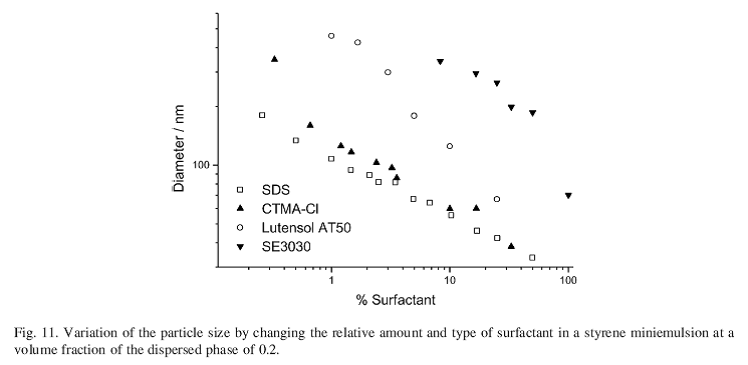
اين به موثرتر بودن پايداري استاتيك نسبت به پايداري استري (steric) مربوط ميشود. يعني براي پايدار كردن استري به مواد بيشتري نياز است. با اين حال اندازه گيري هاي كشش سطحي لاتكسها و تيتراسيون Surfactantها نشان ميدهند كه ذرات غير يوني كاملا باSurfactant پوشيده نشدهاند و كشش سطحي به خوبي بيشتر از لايه هاي اشباع شده با Surfactant است. به علاوه در سيستم هاي غير يوني ميزان پوشش دهي با كاهش اندازه ذرات افزايش مييابد.
براي مطمئنتر شدن از اطلاعات شكل اخیر در مورد بالاتر بودن بازده Surfactantهاي يوني، در صدد برآمديم تا پايداري استاتيك را با افزودن مقادير مختلف نمك كم كنيم. با افزودن NaCl به مينيامولسيون مشخص S/HD اندازه ذرات از 80 به200 nm رسيد.
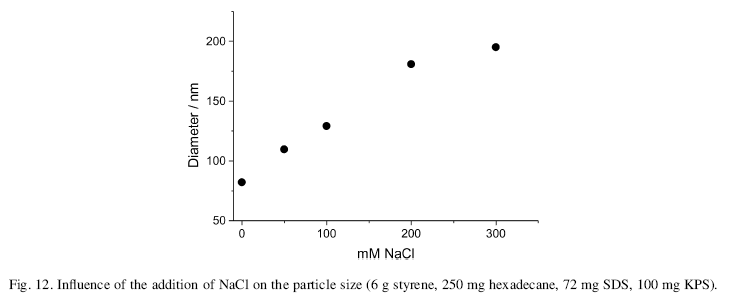
تهيه ي ميني امولسيون از منومر
مينيامولسيونهاي مناسب براي پليمريزاسيون مينيامولسيوني ديسپرسيون هاي منومر در آب به اندازه هاي زير ميكرون هستند كه هم در مقابل افت ناشي از Ostwald ripening و هم تجمع، با يك جزء نامحلول در آب و با وزن مولكولي پايين (Costabilizer) و يك Surfactantمناسب مقاوم شدهاند. نكات كليدي در تهيه ي مينيامولسيون از منومرها روش تهيه و فرمول بندي هستند كه در زير به آنها ميپردازيم.
روش تهيه
شكل زير به طور خلاصه روش تهيه ميني امولسيون ها را نشان ميدهد. سيستم Surfactant در آب و Costabilizer در منومر حل مي شود و همه با هم مخلوط مي شوند. بعد مخلوط تحت يك هموژنايزر با كارايي بالا قرار ميگيرد.
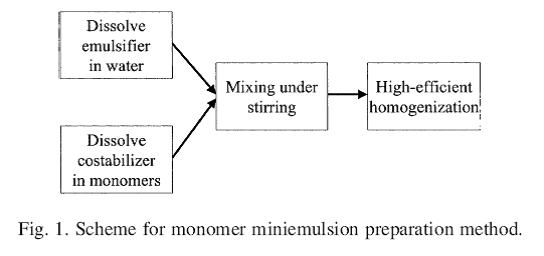
روشهايي ديگري هم گزارش شدهاند. هنگامي كه يك الكل با زنجير طولاني (مانند CA) به عنوان Costabilizer مورد استفاده قرار ميگيرد، الكل و Surfactant ابتدا در آب در دمايي بالاتر از نقطه ذوب الكل هم زده مي شوند. مخلوط تا دماي محيط سرد مي شود و براي از بين بردن فاز ژل مانند، تحت Sonic قرار ميگيرد. بعد در هنگام هم زدن منومر اضافه مي شود و مخلوط حاصل براي مينيامولسيون هموژنيزه، مي شود. اين ايده را ابتدا Ugelstad به كار برد. آنها پي بردند كه الكل مورد نياز براي پايدار كردن سيستم به اين روش كمتر از مقداري است كه ابتدا در منومر حل شود. اما اين روش همانطور كه قبلا هم گفت شد براي مواردي است كه روش هاي هم زدن معمولي به كار ميرود.
Miller نشان داد كه روشي كه اجزا با آن مخلوط ميشوند (قبل از اين كه هموژنيزه شوند) اثري روي سرعت پليمريزاسيون ندارد. اين نشان مي دهد كه تعداد قطرات مينيامولسيوني از نوع اختلاط اوليهي اجزا تاثير نميپذيرد.
اثر آبگريز
قبلا هم گفته شد كه اثر مهاجرت مولكولي Ostwald ripening و ناپايداري نانو قطرات را ميتوان با افزودن آبگريز به فاز ديسپرس شده به خوبي كاهش داد. اين مواد هنگامي كه در فاز آلي قرار ميگيرند، فشار لاپلاس قطرات را خنثي ميكنند. اين جزء بايد مادهاي باشد كه نفوذ آن از قطرهای به قطرهاي ديگر بسيار مشكل باشد و در يك قطره به دام بيفتد. اثر آبگريزها در حفظ پايداري قطرات با مقدار نامحلول آنها در فاز پيوسته افزايش مييابد.
براي آبگریزها از نام Costabilizer هم استفاده ميشود. به كار بردن نام Cosurfactant نادرست است، چون در اغلب موارد اين مواد فعال سطحي نيستند. Cosurfactantها موادي هستند كه فعال سطحي هستند و به همراه Surfactant براي كمتر كردن انرژي بين سطحي به كار ميروند اما به تنهايي نميتوانند تشكيل مايسل بدهند. با به كارگيري مقادير كافي آبگريز و استفاده از يك فرايند هموژنيزاسيون ميتوان به مينيامولسيون پايدار رسيد. بعد از عمل هموژنيزه كردن، بايد يك نوع فرايند تعادل سازي سريع اتفاق بيفتد تا پتانسيل شيميايي در هر قطره، كه ميتواند باعث ايجاد يك فشار باشد، به تعادل برسد. از آن جايي كه تعداد ذرات ثابت هستند، با اين فرايند متوسط اندازه ذرات هم دستخوش تغيير نميشود اما توزيع اندازه ذرات تغيير ميكند. اين فرايند بسيار سريع است و معمولا با آزمايش ثابت نميشود. محاسبه ميشود كه فشار لاپلاس نانوقطره ها و فشار اسمزي (Osmotic) حاصل از آبگريز هنوز به مقدار زيادي از هم فاصله دارند و فشار لاپلاس هنوز به مقدار قابل توجهي از فشار اسمزي بيشتر است.
اگر در بيشترين مقدار اثر Ostwald ripening فشار لاپلاس را با رابطهي PLaplace=2γLL/R محاسبه كنيم (γLL از روش پوشش دهي سطح حاصل مي شود)، 12 بار ميشود. فشار اسمزي كه در خلاف جهت فشار لاپلاس عمل ميكند، از رابطهي Пosm=RTc/M محاسبه ميشود و محاسبهي آن، مقدار 5/4 بار را حاصل ميكند. بنابراين فشار هر قطره كه منجر به پايداري ترموديناميكي ميشود صفر نيست اما مجموع قطرات متعادل هستند. فشار لاپلاس با R-1 تغيير ميكند در حالي كه فشار اسمزي با R-3 تغيير ميكند. بنابراين براي به تعادل رسيدن همه ي قطرات، يك تغيير در اندازه ذرات رخ ميدهد. ولي باعث ميشود كه فشار كل، مقداري مثبت شود. اين باعث ميشود كه سيستم در مقابل تبادل جرم و به تغييرات اندازه ذرات ايمن شود. مشاهده ي يك آزمايش نشان ميدهد كه انداره ذرات مينيامولسيونهاي پايدار شده، بعد از مدت زماني طولاني (در مقياس 100 ساعت) بزرگ ميشوند تا به فشار خالص (PLaplace- Пosm) صفر شود.
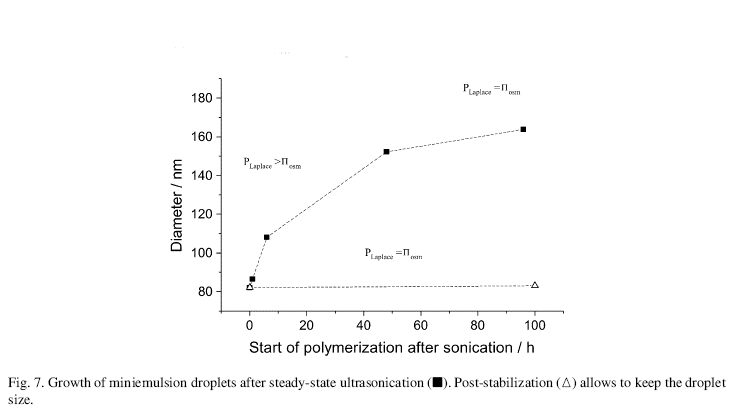
ميتوان با افزودن مقداري Surfactant بعد از مرحله ديسپرسيون پايداري را بيشتر كرد. اين مقدار Surfactant براي كوچكتر كردن اندازه ذرات نيست. بلكه به نواحي خالي نانو قطره ها جذب ميشوند و سطح تماس آب و روغن را كاهش ميدهند و در نتيجه فشار لاپلاس هم كمتر ميشود. اين مينيامولسيون ها بعد از ساعتها و حتي ماه ها پايدار ميمانند. به لحاظ ترموديناميكي پايدار هستند و پتانسيل شيميايي قطرات، مينيمم و براي وقوع واكنشهاي شيميايي مناسب هستند.
اندازه ذرات قطراتي كه به سرعت پليمريزه ميشوند، به مقدار آبگريز ربطي ندارد و يا رابطهي ضعيفي دارد. يعني اينطور نيست كه وقتي مقدار آبگريز دو برابر شود، اندازه ذرات نصف شوند. فشار موثر (اختلاف فشار لاپلاس و اسمزي) بايد در همه ي قطرات يكسان باشد. حداقل مقدار آبگريز نسبت به منومر (نسبت مولي 1به 250) مورد نياز است تا فشار اسمزي كافي حاصل شود.
مشاهده شده كه مقادير اندك از مواد با جرم مولكولي بالا مانند پلياستايرن ميتواند در پايدار سازي كمك كند. اما اين پايداري فقط در مرحلهي پليمريزاسيون است. يك تست ديگر براي اثبات "فشار موثر برابر" ، به اين صورت است: دو مينيامولسيون با مواد مشابه و با مقادير مختلف آبگريز، با هم مخلوط شدند. قطرات با مقدار كمتر آبگريز كوچكتر شدند و قطراتي كه مقدار بيشتري آبگريز داشتند بزرگ شدند تا زماني كه پتانسيل همهي قطرات يكسان شدند. يك ديسپرسيون با دو اندازه ذره حاصل شد ولي تعداد قطرات تغييري نكرد.
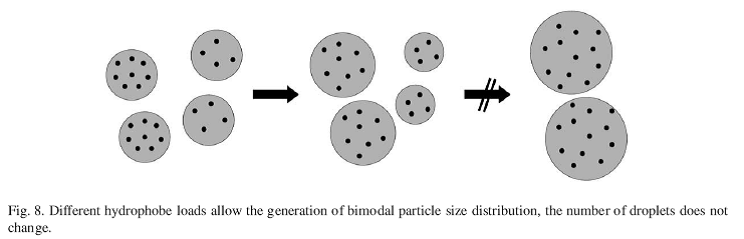
انتخاب آبگريزها بسيار گسترده است. HD، Dyeهاي آبگريز، كومنومرها، پلاستي سايزرها، افزودني هاي ديگر مي توانند استفاده شوند. سيلانها سيلوكسانها، ايزوسيانات ها، پلياستر و آلكانهاي فلوئوردار هم در جلوگيري از Ostwald ripening موثر هستند. بديهي است كه هر چه تركيب، قابليت انحلال كمتري داشته باشد، مي تواند فشار اسمزي بيشتري توليد كند.
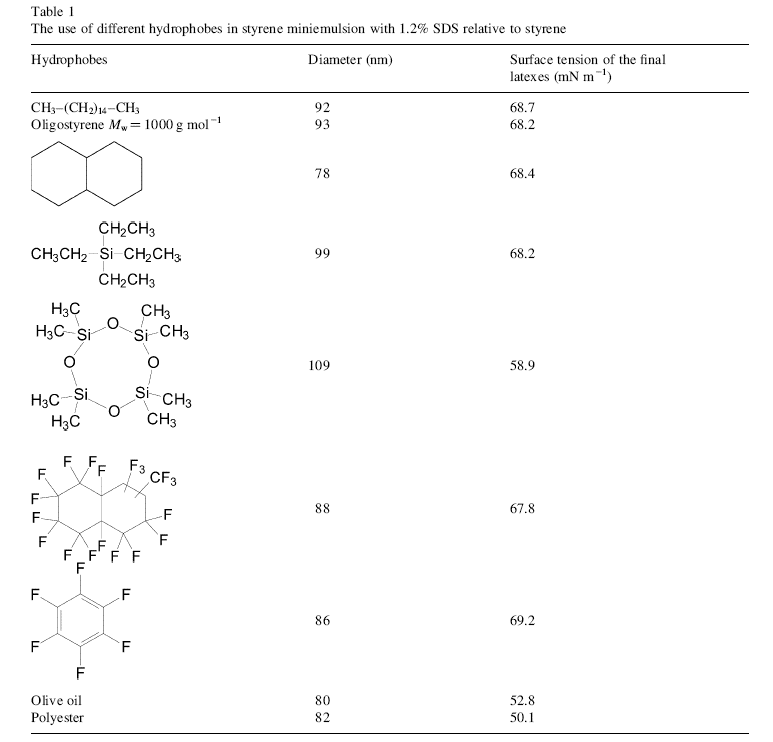
Ugelstad نشان داد كه با افزايش طول زنجيره هاي آبگريز، پايداري مينيامولسيون افزايش پيدا مي كند. Delgado گزارش داد كه نسبتHD/SDS با نسبت مولي 1 به 4، پايداري خوبي ايجاد ميكند. كه در برخي موارد رد شد. به هر حال چون HD با SDS در سطح قرار نميگيرد و در داخل قطرات است، پيدا كردن نسبت بهينه آن با SDS غير ضروري به نظر ميرسد. Fontento جزئيات استفاده از پليمر به عنوان آبگريز را توضيح داد. پليمرها به خاطر سازگاري با منومرها و آبگريزي، در بسياري از موارد گزينه هاي مناسبي هستند. نشاد داده شد كه استفاده از پليمرها به عنوان آبگريز پايداري خوبي براي پليمريزاسيون ايجاد ميكند. Rumers گفت كه پليمريزاسيون مينيامولسيوني با افزودن پليمر و يا ذرات ورم كرده پليمر، نتايج يكساني ميدهد. انتقال جرم بين قطرهاي (بين ذرهاي) با نيروي محركه ترموديناميكي كنترل ميشود كه مربوط به انرژي بين سطحي و انرژيهاي هم زدن و تغيير شكل الاستيكي ذره هاي حاوي پليمر، عامل ورم كننده و يا آبگريز است. اغلب امولسيونها، به لحاظ ترموديناميكي ناپايدار هستند اما ميتوان گفت كه به لحاظ سينتيكي پايدار هستند. يعني اثرات مخرب مثلا Ostwald ripening به اندازهاي كند هستند كه قبل از اين كه مشكلي ايجاد شود، هسته سازي و پليمريزاسيون رخ ميدهد. يك گزينه ديگر كه همزمان به صورت آبگريز و كوسرفكتانت عمل ميكند، الكلهاي زنجيره بلند است. اضافه كردن CA به يك سيستم SDS/آب/روغن، پايداري را نسبت به حالت SDS تنها افزايش ميدهد. كشش سطحي بين آب و استايرن در حضور مخلوط Surfactantها (SDS/CA و يا CA/CTMA)، بين 5 تا 13 mNm-1تخمين زده شد. در حالي كه انرژي سطحي ظاهري بين فاز آبي و لايهي بين سطحي حاصله، كمتر از 1 mNm-1 بود. يعني با زياد شدن طول زنجير الكل، كشش سطحي هم زياد ميشود.
Lack خواص بين سطحي Cetyl يا Lauryl الكل را بررسي كرد و به اين نتيجه رسيد كه پايداري حاصل از CA فقط به خاطر جلوگيري از نفوذ مولكولي نيست. از آنجایي كه CA كشش سطحي را تحت تاثير قرار ميدهد، به نظر ميرسد كه بيشتر به عنوان Cosurfactant عمل ميكند (همانند چيزي كه در ميكروامولسيونها نشان داده شده) تا آبگريز.
Ugelstad و Chou بهترين پايداري مينيامولسيون استايرن را در نسبت مولي Surfactant يوني به CA 1 به 1 و 1 به 3 به دست آوردند.Brouwer اثر حلاليت فاز ديسپرس شده را بر روي مينيامولسيون حاصل از پخش روغن در فاز ژلي با استفاده از هم زدن ساده بررسي كرد. وي به اين نتيجه رسيد كه با بيشتر شدن حلاليت، ميني امولسيون با CA راحتتر تهيه ميشود. اما پايداري كلي آن كاهش مييابد. Ugelstadنشان داد كه وقتي كه طول زنجير Costabilizer يا آبگريز افزايش ميبابد، پايداري مينيامولسيون زياد ميشود. Choi اثر طول زنجير الكل و اثر نسبت الكل بلند زنجیر (CA) به SDS به پايداري را، با سانتريفيوژ كردن روغن ديسپرس شده و زمان دادن به آن بررسي كرد. بهترين نتيجه در نسبت CA به SDS، 1 به 3 حاصل شد. و پايداري با ازدياد طول زنجبر الكل چرب افزايش يافت. در مورد CA افزودن مقداري پليمر، فشار اسمزي را زياد ميكند و پايداري زياد ميشود. HD و CA براي كاربرد هاي تجارتي نامطلوب هستند. بنابراين اقسام ديگري از آبگريز ها به كار گرفته شدند. براي مثال dodecyl mecaptane (DDM) به عنوان آبگريز و عامل انتقال زنجير عمل ميكند. مينيامولسيونها با DDM پايداري زيادي را از خود نشان ميدهند. چون آن ها اثر Ostwald ripening را كاهش ميدهند. مينيامولسيون نسبتا پايدار استايرن با استفاده ازDye آبي (Blue 70) آبگريز، با وزن مولكولي پايين حاصل شد.
كومنومرهاي نامحلول هم ميتوانند پايداري خوبي در مقابل نفوذ مولكولي به قطرات بدهند. مينيامولسيونهاي استايرن را ميتوان با آبگريزهاي فعال پايدار كرد. اثربخشي اين آبگريزها، به ميزان حلاليت آنها بستگي دارد. هر چه آبگريز به ميزان بيشتري در آب قابل حل باشد،Ostwald ripening بيشتر ميشود. ميزان انحلال پذيري به اين صورت است: CA>DMA>SMA>HD. در مورد DMA، هم اثر نفوذ مولكولي و هم ويسكوز شدن (craming) در دماي 35 درجه سلسيوس ديده ميشود. در حالي كه براي مينيامولسيونهاي حاوي SMA اين طور نيست. قابليت آغازگرهايي با قابليت انحلال خيلي كم مانند Lauryl peroxide (LPO) در حفظ پايداري قطرات منومري و جلوگيري از اثر نفوذ مولكولي بررسي شد و نتايج با Benzoyl peroxide (BPO) و AIBN مقايسه شد و مشاهده شد كه تنها LPO مناسب است. پليمريزاسيون مينيامولسيوني با استفاده از LPO به عنوان آبگريز انجام شد و نتيجه اين بود كه به اندازه کافی و تا زماني كه پليمريزاسيون آغاز شود، پايدار ميماند. اندازهگيريهاي پايداري استايرن با استفاده از پايداري Shelf-Life و سانتريفيوژ شديد انجام شد.
اندازه گيري ذرات
اندازه گيري ذرات پليمر را ميتوان به راحتي به روش پخش نور (Light scattering) و يا روشهاي ميكروسكوپي انجام داد. چون كه ديسپرسيون ها به راحتي بدون تغيير اندازه ذرات رقيق ميشوند.
Ugelstad از TEM استفاده كرد. Goetz و El-Aassar از تكنيكهاي انتشار نور و TEM استفاده كردند. Miller با استفاده از CHDF مشاهده كرد كه در سيستم هاي CA در يك بازهي زمان اندازه ذرات به سرعت افزايش مييابند و بعد از آن، افزايش اندازه ذرات به آهستگي صورت ميگيرد. اين مشاهده در مورد سيستم هاي HD ديده نشد. براي آن اندازهگيريها بايد امولسيون را رقيق كرد كه شديدا روي سيستم تغيير ايجاد ميكند. حتي اگر با آب اشباع شده از منومر هم رقيق سازي انجام شود، به دليل تفاوت در انحلال پذيري، تغييري اندك در اندازه ذرات رخ ميدهد. برش اعمال شده در روش CHDF هم ميتواند باعث لخته شدن قطرات شود.
اندازه گيري خواص قطرات امولسيونها در محيطهاي غليظ كار مشكلي است. برخي از روشهاي غير مستقيم به كار رفتند. مساحت بين سطحي و اندازه ذرات در مينيامولسيون (آب/SDS/SMA/استايرن) و امولسيون (استايرن/SDS/آب) اندازهگيري شده، با هم مقايسه شدند.
Erden، اندازه ذرات در مينيامولسيون غليظ را با تيتراسيون صابون، اندازهگيري كرد و نتايج را با CHDF چك كرد. اندازه ذرات، بدون رقيق كردن سيستم ميتوانند با SANS هم اندازهگيري شوند. در اين روش سيستم شامل قطرات روغن در آب پروتونه شده است تا Scattering contrast زيادي داشته باشند.
اندازه گيري فرايندهاي انتقال انجام شده بين قطرات در فاز آبي هم موضوع برخي از مقالات است. جابجايي و تبادل روغن بدون هيچ تاثيري بر روي اندازه ذرات نهايي، انتقال تعادلي با جبراني (Compensated transfer) ناميده ميشود. انتقال هاي غيرتعادلي، مكانيزمهاي اصلي پديده Ostwald ripening و لخته شدن هستند. انتقالهاي غير تعادلي با افزودن آبگريز جلوگيري ميشوند. اما انتقالهاي تعادلي همچنان ادامه مييابند. در يك مخلوط حاوي قطرات دو امولسيون (يكي tetradecane و ديگري 1-bromo tetradecane) نشان داده شد كه انتقالهاي تعادلي بسيار سريع تر از چيزي هستند كه در Ostwald ripening رخ ميدهند. دو مينيامولسيون يكي حاوي MMA و ديگري استايرن به كار رفته اند كه نشان بدهند منومرها از يك قطره به قطره ديگر انتقال مييابند كه البته ابن انتقال ممكن است به خاطر پتانسيل شيميايي متفاوت قطرات باشد.
در جداول زیر کارهای انجام شده بر روی مینیامولسیونها به اختصار آورده شده است:
منبع:
- Jose M. Asua, Miniemulsion polymerization, Institute for Polymer Materials (POLYMAT) and Grupo de Ingenierta Qutmica, Facultad de Ciencias Qufmicas, The University of the Basque Cmmtry, Apdo 1072, 20080 Donostia-San Sebastian, Spain, Progress in polymer science, 2002
- Markus Antonietti, Katharina Landfester, Polyreactions in miniemulsions, Max Planck Institude of Colloids and Interfaces, Research campus Golm, D-14424 Potsdam, Germany, Progress in polymer science, 2001
- Jianli Wang, Zhongjie Du, Congju Li, Hangquan Li, Chen Zhang, A Study on Formation and Stability of Epoxy Resin Inverse Concentrated Water/Oil Emulsion, The Key Laboratory of Beijing City on Preparation and Processing of Novel Polymer Materials, Beijing University of Chemical Technology, Beijing 100029, People’s Republic of China, Wiley InterScience, 2008
- Frederick H. Walker, John B. Dickenson, Charles R. Hegedus, Frank R. Pepe, Cationic polymerization of emulsified epoxy resins, Air Products and Chemicals, Inc., 7201 Hamilton Blvd., Allentown, PA 18195-1501, USA, Progress in organic coatings, 2002
- Zhenzhong Yang, Delu Zhao, Mao Xu, Yuanze Xu, Mechanistic investigation on the formation of epoxy resin multi-hollow spheres prepared by a phase inversion emulsification technique, Polymer Physics Laboratory, Center for Molecular Science, Institute of Chemistry, The Chinese Academy of Sciences,
Beijing 100080, China, Marcomolecular rapin Communications, 2000
- Kenichi Hibino, Yoshiharu Kimura, Particle Formation of Epoxy Resin in Aqueous Emulsion State, EC Intracorporation, Sanyo Chemical Industries, Ltd., 11-1 Ikkyonomoto-cho, Higashiyama-ku, Kyoto 605-0995, Japan, Marcomolecular materials and engineerin, 2001
- HIDEAKI KAWAHARA, TOKIO GOTO, KIYOSHI OHNISHI, HIRONAO OGURA, HIROYUKI KAGE, YOSHIZO MATSUNO, Preparation of Epoxy Resin/Acrylic Composite Latexes by Miniemulsion Polymerization Method, Kansai R&D Center, Dainippon Ink & Chemicals, Inc., 1-3, Takasago, Takaishi, Osaka 592-0001, Japan, 2000
- Zhang Zhaoying, Huang Yuhui , Liao Bing, Cong Guanglning, Studies on particle size of waterborneemulsions derived from epoxy resin, G!langzllOu Institute of Chemistry, Chinese Academy of Sciences, Guangzhou 510650, People's Republic of China, European Polymer Journal, 2000
A 103: polyoxyethylenated nonylphenol half ester of sulphosuccinic acid;
AA: acrylic acid;
Alipal CO-436: ammonium salt of sulfated nonylphenoxy poly(ethylenoxy) ethanol;
AMBN: 2,2'-azobis(2-methylbutyronitrile);
BA: buryl arylate;
Brij 35: CI2H25-O-(C2H4O)23;
CA: cetyl alcohol;
DDM: dodecyl mercaptane;
DMA: dodecyl methacrylate;
DMAEMA: dimethyl amino ethyl methacrylate;
Dowfax 8390: disulfonated alkyl diphenyl oxid Sodium salt;
EHA: ethylhexyl acrylate;
EHMA: ethylhexyl methacylate;
HD: hexadecane;
LPO: lauroyl peroxide;
MAA: methacrylic acid;
miniEP: miniemulsion polymerization;
MMA: methyl methacrylate;
n-DM: n-dodecyl mercaptan;
NP-40: nonyl polyethoxylate with 40 EOs per molecule;
NE-40: polymerizable nonyl polyethoxylate with 40 EOs per molecule;
OPB: octadecyl pyridinium bromide;
PB/Et-co-PEO: poly(butylene/ethylene-co-ethyleneoxide);
PMMA: poly(methyl methacrylate);
pMMA-b-DMAEMA: poly(methyl methacrylate-b-2-(dimethylamino) ethyl methacrylate block copolymer;
PS: polystyrene;
PVOH: polyvinyl alcohol;
S: styrene;
SDS: sodium dodecyl sulfate;
SHS: sodium hexadecyl sulfate;
SLS: sodium lauryl sulfate;
SMA: stearyl methacrylate;
VAc: vinyl acetate;
VC: vinyl chloride;
?: not disclosed








